Elektronisk konfiguration - atomernas struktur hemligheter
På hösten 1910, Ernst Rutherford,meditera, försökte förstå atomens inre struktur. Hans experiment på spridningen av alfapartiklar av olika ämnen bevisade övertygande - inuti atomen finns det en del massiv kropp, hittills obefogad. År 1912 skulle Rutherford kalla det atomkärnan. I vetenskapens huvud svängde tusentals frågor. Vad är ansvaret för denna okända kropp? Hur många elektroner behövs för att säkerställa dess vikt?
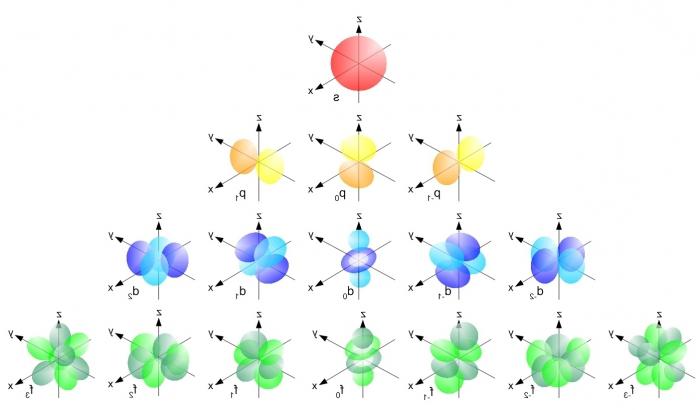
I maj 1911 publicerade Rutherford en artikel omatomstruktur som föregår mycket viktig varning att stabiliteten för den atomära strukturen är sannolikt att bero på nyanser i den inre strukturen av atomen och rörelsen av laddade partiklar som är dess huvudsakliga strukturella komponenten. Så den elektroniska konfigurationen föddes - den atom-elektroniska atommodellen. Denna modell var avsedd att spela en ovärderlig roll i kärnfysiken.

Elektronisk konfiguration är ordningenfördelningen av elektroner över atomomgångar. Tack vare den nyfiket sinne och uthållighet Ernest Rutherford, som kunde försvara sin idé, har vetenskapen har berikats med ny kunskap, vars betydelse kan inte nog understrykas.
Den elektroniska konfigurationen av atomen är som följer. I mitten av hela strukturen är en kärna bestående av ett annat antal neutroner och protoner för varje substans. Vad bestämmer kärnans positiva laddning. Runt det i motsvarande koncentriska banor flyttar elektroner - negativt laddade elementära partiklar. Dessa atomomgångar kallas också skal. Den yttre omloppet av en atom kallas valens. Och antalet elektroner på det är valens.
Varje elektronisk konfiguration av elementenskiljer sig från antalet elektroner som finns i den. Till exempel, en mycket enkel sak i universum - väte - innehållande endast en enda elektron, syreatom, - åtta och elektronkonfiguration järn har tjugo sex elektroner.
Men det bestämda värdet i den elektroniska modellenAtomen har inte antalet elektroner alls, men vad håller dem ihop och gör hela systemet funktionellt - kärnan och dess sammansättning. Det är kärnan som ger substansen sina individuella egenskaper och egenskaper. Elektroner lämnar ibland atommodellen, och sedan förvärvar atomen en positiv laddning (tack vare kärnladdning). I detta fall ändras inte substansen av egenskaperna. Men om du ändrar kärnans sammansättning blir det en helt annan substans med olika egenskaper. Det här är inte lätt, men det är fortfarande möjligt.

Eftersom den elektroniska konfigurationen är omöjlig utandess huvudsakliga strukturella element - atomkärnan, det bör ägna särskild uppmärksamhet. Det är detta centrala element i den atommodell som bildar de enskilda egenskaperna och egenskaperna hos varje kemisk substans. Protoner, som i själva verket ger kärnan en positiv laddning, är 1840 gånger tyngre än någon elektron. Men kraften hos laddning av en proton är lika med den hos någon elektron. I ett tillstånd av balans är antalet protoner i en atom lika med antalet elektroner. I detta fall är kärnan bäraren av nollladdningen.
En annan viktig partikel i atomkärnan kallas en neutron. Det är detta element som inte har någon avgift som möjliggjorde en kedjekärnreaktion. Så det är helt enkelt omöjligt att överskatta värdet av en neutron.







